Швейцарские ученые обнаружили, что окисленный никотинамидадениндинуклеотид (НАД+) управляет процессом старения стволовых клеток, действуя на активность митохондрий. В эксперименте назначение биологического предшественника НАД никотинамидрибозида (НР) мышам улучшило состояние их мышечных, нервных и пигментных стволовых клеток, что увеличило продолжительность жизни животных. При этом НР представляет собой ничто иное как производное ниацина, или витамина В3. В другом исследовании американский научный коллектив определил концентрацию НАД в разных клеточных структурах и выявил механизмы ее поддержания в митохондриях. Отчеты о работах и экспертный комментарий к ним опубликованы в журнале Science.
Сотрудники Федеральной политехнической школы в Лозанне с коллегами сравнили экспрессию генов в мышечных стволовых клетках молодых (около трех месяцев) и пожилых (около 24 месяцев) мышей. Они выяснили, что наиболее сильно при старении снижается активность митохондриальных генов цикла трикарбоновых кислот и окислительного фосфорилирования. Эти процессы тканевого дыхания обеспечивают клетку энергией в виде АТФ. Дисфункцию митохондрий подтвердило также непосредственное выявление снижения их мембранного потенциала, уменьшение уровня дыхания и истощение клеточных запасов АТФ. Также при старении снижалась экспрессия генов сигнального пути стрессорного ответа UPRmt, который обеспечивает адаптацию митохондрий, и генов клеточного цикла. При этом повышалась экспрессия генов старческого воспалительного секретома клеток.
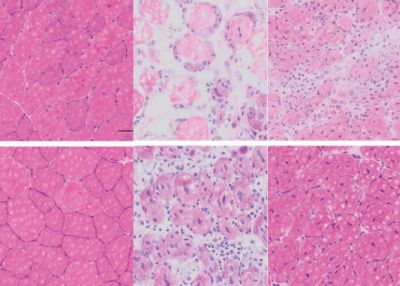
Также ученые убедились, что в стволовых клетках пожилых мышей снижена концентрация НАД+. Этот кофактор окислительно-восстановительных ферментов, служащий переносчиком электронов, необходим для работы митохондрий, ядра и других клеточных структур. Шестинедельный курс НР повысил концентрацию НАД+ в мышечных стволовых клетках и молодых, и пожилых мышей, и увеличил их количество в мышцах. Кроме того, у мышей старшего возраста препарат независимо от стволовых клеток улучшил функцию мышц, действуя непосредственно на их волокна. Положительное влияние НР на состояние мышечной ткани подтвердили у животных с токсическим повреждением мускулатуры и трансгенных животных с мышечной дистрофией.
Иммунохимический анализ и электрофорез на геле выявили в клетках пролеченных пожилых мышей уменьшение уровней маркеров возрастных повреждений ДНК — разрывов цепей, фофорилирования гистона 2A.X и бета-галактозидазы. Также в клетках снизилось содержание мРНК, кодирующих циклинзависимый ингибитор киназы 1 типа (CDKN1A) и связанных с ним провоспалительных белков. При этом повысилась экспрессия ферментов окислительного фосфорилирования и пути UPRmt, а также белков клеточного цикла, увеличились мембранный потенциал митохондрий и концентрация АТФ в клетке. Опыты с трансгенными мышами показали, что положительный эффект терапии связан с ее действием на сиртуин-1 — НАД+-зависимую деацилазу, стимулирующую биогенез митохондрий. Также ученые выяснили, что повышение уровня белков UPRmt и клеточного цикла обусловлено тем, что НР стимулирует экспрессию прогибитинов, реагирующих на митохондриальный стресс. Изучение других тканей до и после курса НР показало, что препарат повышает пролиферацию нервных стволовых клеток в мозге и предотвращает возрастное уменьшение числа меланоцитов в волосяных фолликулах.
Также НР
вызывал небольшое, но значимое увеличение средней продолжительности жизни
пожилых мышей (868 против 829 дней в контрольной группе). По мнению исследователей,
слабо выраженное действие препарата на продолжительность жизни связано с тем,
что его назначали животным, уже достигшим пожилого возраста (24 месяца). Это
значит, что процесс старения может быть отчасти обусловлен нарушением гомеостаза
НАД+ в стволовых клетках, заключили авторы работы.
Группа ученых из Орегонского университета здоровья и наук уточнила распределение НАД+ в разных клеточных структурах. Для этого они создали количественный молекулярный сенсор, состоящий из флуоресцирующего белка Venus и НАД+-связывающего домена бактериальной ДНК-лигазы. С его помощью они выяснили, что содержание кофермента примерно соответствует константе Михаэлиса для поли(АДФ-рибоза)-полимеразы (PARP) в ядре и сиртуинов в митохондриях. Это свидетельствует о том, что концентрация НАД+ регулирует активность указанных ферментов в соответствующих клеточных структурах. Дальнейшие эксперименты с выключением ферментов семейства NMNAT, синтезирующих НАД+, показали, что митохондрии имеют по меньшей мере два источника этого кофермента. Они могут как получать его из цитоплазмы, так и синтезировать самостоятельно.
Значение НАД+ для функционирования митохондрий и, как следствие, для контроля клеточного старения делает направленные на его метаболизм лечебные методики потенциальным способом продления жизни. Однако для этого необходимо подтвердить полученные результаты в исследованиях на людях, а также разработать оптимальные схемы терапии.
Олег Лищук